В биомедицине, где приоритетом является высокая точность анализа и неукоснительное соблюдение стандартов качества, ключевое значение приобретает объективная оценка микроструктуры, топографии поверхности, элементного распределения и фазового состава лекарственных средств. Эти параметры служат фундаментом для понимания физико-химических свойств препаратов, подтверждения их терапевтической эффективности, безопасности и воспроизводимости от партии к партии.
Сканирующий электронный микроскоп (СЭМ), обладающий разрешающей способностью на субмикронном уровне, позволяет детально изучать межфазные границы между активным фармацевтическим ингредиентом (АФИ) и вспомогательными компонентами, особенности пористой архитектуры и кристалломорфологические характеристики. Полученные данные служат основой для объяснения профилей высвобождения твердых лекарственных форм, расшифровки механизмов пролонгированного действия и рационального выбора технологических параметров. Таким образом, СЭМ выступает связующим звеном между микроструктурой и макроскопическими характеристиками препарата, обеспечивая научную поддержку при создании инновационных лекарственных форм и мониторинге их качества.
1. Ключевые направления применения в контроле качества лекарств
Макроскопические свойства твердых лекарственных форм зачастую напрямую определяются особенностями их микрорельефа. Любые дефекты поверхности, инородные включения или следы загрязнений могут негативно сказаться на стабильности, скорости высвобождения и, в конечном счете, на безопасности препарата. Основная ценность СЭМ здесь заключается в его способности к высокоточному морфологическому анализу.
Оценка качества покрытия и выявление дефектов поверхности
Для таблетированных форм однородность оболочки, отсутствие трещин, эффекта «апельсиновой корки» или отслоений — важнейшие критерии технологического совершенства. Использование СЭМ в режиме анализа поперечных срезов позволяет количественно оценить толщину покрытия, изучить адгезию между оболочкой и ядром, а также выявить внутреннюю пористость. Например, для кишечнорастворимых таблеток целостность покрытия является определяющим фактором, обеспечивающим прохождение через желудок и последующее высвобождение в тонком кишечнике.
Идентификация инородных включений и контаминантов.
Микроскопические частицы металла, фрагменты полимеров, текстильные волокна — подобные загрязнения, попадающие в продукт в ходе производства, представляют собой серьезную угрозу для качества.
Высокое разрешение СЭМ позволяет не только локализовать такие включения, но и определить их морфологию, что критически важно для установления источника контаминации.
Так, при плановой проверке качества капсул с сульфатом глюкозамина с помощью оптического микроскопа были обнаружены мелкие дефекты на поверхности. Последующий анализ на СЭМ при высоком увеличении выявил микротрещины и прикрепленные пластинчатые частицы неправильной формы (рис. 1а). Морфология трещин указывала на их возможное происхождение в результате коррозии под напряжением, связанной с неравномерной сушкой покрытия и релаксацией полимерных напряжений. Инородные частицы по своей структуре (рис. 1b — чистая поверхность) отличались от матрицы капсулы.
Сопоставление с типичными микроорганизмами позволило исключить биологическую природу загрязнения; наиболее вероятным источником была признана неорганическая пыль из производственной среды или вспомогательных веществ. Эти данные послужили основой для корректировки режимов нанесения покрытия и ужесточения контроля чистоты в производственных помещениях.


Рис. 1а — Поверхность капсулы с сульфатом глюкозамина: визуализированы пластинчатые включения и микротрещины; загрязнения проникают в трещины. Изображения получены с помощью микроскопа LANSEM 30.
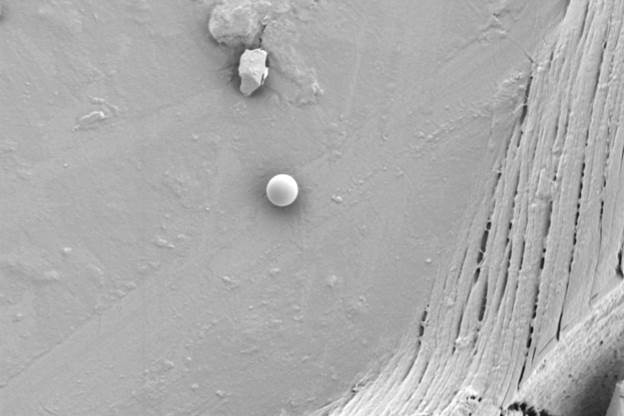
Рис. 1b — Фрагмент неповрежденной поверхности капсулы (без загрязнений). Изображение получено с помощью LANSEM 30.
2. Преимущества метода при исследовании микроструктуры фармацевтических субстанций и готовых форм
Микроструктурные параметры – кристалломорфология, поровое пространство, характер распределения компонентов – напрямую влияют на скорость растворения и, следовательно, на биодоступность. СЭМ предоставляет уникальные возможности для изучения этих параметров.
Анализ активных фармацевтических ингредиентов.
Метод позволяет наглядно дифференцировать полиморфные модификации одного и того же вещества, которые могут различаться по растворимости и стабильности. Длительное наблюдение за АФИ в различных условиях с помощью СЭМ помогает оценить стабильность полиморфной формы и обосновать выбор состава и технологии.
Исследование сложных лекарственных форм.
Для систем с модифицированным высвобождением СЭМ раскрывает взаимосвязь между внутренней архитектурой и кинетикой высвобождения. Например, хлорид калия в исходном состоянии характеризуется кубической кристаллической решеткой (рис. 2а).
При разработке таблеток с пролонгированным высвобождением на основе гидроксипропилметилцеллюлозы (ГПМЦ) методом СЭМ было установлено, что измельченные частицы хлорида калия (сохраняющие фрагменты кубической формы) равномерно распределены и прочно связаны непрерывной гелевой матрицей ГПМЦ. Граница раздела фаз характеризуется хорошей адгезией, структура отличается плотностью и низкой пористостью (рис. 2b). Такая плотная упаковка замедляет проникновение жидкости и обеспечивает диффузионно-контролируемое высвобождение, что согласуется с моделью Хигучи – математическим уравнением, описывающим высвобождение лекарственного вещества из твердой матричной системы.
Другой пример — сравнительный анализ таблеток метформина с немедленным и пролонгированным высвобождением. СЭМ-изображения показывают, что немедленная форма имеет рыхлую структуру: между частицами АФИ и вспомогательными веществами присутствуют многочисленные поры и слабые контакты, что способствует быстрому проникновению растворителя и ускоренному растворению (рис. 3а).
Напротив, в пролонгированной форме частицы АФИ инкапсулированы плотной трехмерной гелевой сеткой полимера (рис. 3b), которая удлиняет путь диффузии и увеличивает сопротивление массопереносу. Выявленные структурные различия напрямую объясняют разницу в фармакокинетических профилях.

Рис. 2а — Кубические кристаллы хлорида калия.

Рис. 2b — Таблетка хлорида калия с пролонгированным высвобождением: частицы АФИ (сохранившие части кубической огранки) интегрированы в плотную гелевую матрицу ГПМЦ. Изображение получено с помощью СЭМ LANSEM 30.

Рис. 3а — Таблетка метформина с немедленным высвобождением: рыхлая упаковка, развитая пористость. Изображение получено с помощью LANSEM 30.

Рис. 3b — Таблетка метформина с пролонгированным высвобождением: частицы АФИ заключены в непрерывную плотную полимерную сеть. Изображение получено с помощью микроскопа LANSEM 30.
3. Поддержка при оптимизации технологических процессов
В современной фармацевтической парадигме «качество закладывается при разработке» (Quality by Design, QbD) СЭМ выступает инструментом, предоставляющим наглядные микроструктурные доказательства для обоснования технологических решений.
Инженерия частиц.
С помощью настольного сканирующего микроскопа (СЭМ) можно детально охарактеризовать распределение частиц по размерам, их форму и состояние поверхности как для АФИ, так и для вспомогательных веществ. Эти параметры непосредственно влияют на сыпучесть, прессуемость и однородность смеси, а следовательно, относятся к критическим атрибутам качества, подлежащим строгому контролю.
На примере гранул витамина B1 и детских гранул парацетамола + хлорфенирамина малеата СЭМ позволяет визуализировать различия в морфологии. Гранулы витамина B1 характеризуются узким распределением по размерам и сферической формой, что свидетельствует о корректно подобранных параметрах распылительной сушки и обеспечивает хорошую сыпучесть (рис. 4).
В случае детских гранул при увеличении обнаруживаются нитевидные структуры, прочно прикрепленные к поверхности (рис. 5). Подобные образования могут возникать из-за неоптимальной скорости испарения растворителя, вызывающей миграцию и кристаллизацию компонентов. Полученные микрофотографии дают четкое направление для совершенствования режима сушки.
Разработка систем доставки.
Вне зависимости от типа — микросферы, наночастицы или сложные композиты — СЭМ обеспечивает детальную визуализацию их морфологии, необходимую для понимания механизмов действия и оптимизации получения.
Таким образом, сканирующая электронная микроскопия является незаменимым инструментом на всех этапах жизненного цикла лекарственного средства: от изучения субстанции и разработки состава до контроля производства и оценки качества.
Информация о морфологии, получаемая с помощью СЭМ, служит надежной основой для рационального конструирования препаратов и повышения их эффективности и безопасности. По мере ужесточения требований к качеству фармацевтической продукции роль сканирующих электронных микроскопов (СЭМ) будет только возрастать, открывая новые возможности для разработки и контроля современных лекарственных форм.

Рис. 4 — Гранулы тиамина (витамин B1): однородные, сферические, демонстрируют хорошую сыпучесть. Изображение получено с помощью LANSEM 30.

Рис. 5 — Детские гранулы парацетамола и хлорфенирамина малеата: на поверхности видны нитевидные структуры, образовавшиеся в процессе сушки. Изображение получено с помощью LANSEM 30.
Компания «СИНЕРКОН» успешно внедряет современные настольные сканирующие электронные микроскопы, предлагая лабораториям и производственным предприятиям комплексное решение для высокоточного микроструктурного и элементного анализа. Мы обеспечиваем полное методическое и техническое сопровождение: от предварительного подбора конфигурации и пусконаладочных работ до профессионального обучения специалистов.
В демонстрационном зале «СИНЕРКОН» установлен действующий настольный СЭМ, где по предварительной записи вы можете протестировать собственные образцы и лично убедиться в том, что оборудование эффективно решает ваши аналитические задачи. Благодаря оптимизированной логистике и наличию оборудования на складе мы гарантируем быстрые сроки поставки и оперативное внедрение микроскопов в рабочий процесс.
Дополнительно компания предоставляет расширенное гарантийное и квалифицированное постгарантийное обслуживание, включая оперативную техническую поддержку и поставку расходных материалов, что позволяет нашим клиентам сосредоточиться на исследованиях, будучи уверенными в стабильной работе оборудования на протяжении всего жизненного цикла.